| |
 |
|
|
|
| |
Dr Ben Bradshaw
Secció de Química Orgànica, planta 2, edifici B, despatx 14
benbradshaw@ub.edu |
|
|
|
| |
Apunts de Classe (Grup M2) |
|
|
|
| |
|
|
|
|
| |
 |
|
|
|
| |
TEMA 1.1: Reaccions orgàniques: conceptes generals |
|
|
|
| |
 |
|
|
|
| |
Classe: 1.01: Introducció General |
|
|
|
| |
Una introducció al curs. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Introduïr el material del curs disponible i explicar la millor manera de superar el curs amb èxit.
Enllaços a recursos introduïts: mapa sintètic |
|
|
|
| |
Resum de Classe 1.01 |
|
|
|
| |
 |
|
|
|
| |
Classe: 1.02: Els fonaments de la reactivitat orgànica |
|
|
|
| |
En aquesta classe introductòria parlarem d'un dels conceptes més fonamentals necessaris per a la química orgànica: el de les reaccions entre nucleòfils i electròfils per fer nous enllaços químics. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Demostra com funciona la reactivitat entre molècules mitjançant una demostració interactiva senzilla. Mostra com hem de dividir els reactius en 2 classes segons siguin rics en electrons (nucleòfils) o deficients en electrons (electròfils). Il·lustrar com sintetitzar una molècula invertint el procés explicat anteriorment |
|
|
|
| |
Resum de Classe 1.02 |
|
|
|
| |
 |
|
|
|
| |
Classe 1.03: Revisió de Conceptes Àcid-Base: El Model M.A.R.I.O. |
|
|
|
| |
Les reaccions àcid-base són un component clau de moltes reaccions orgàniques. Com a resultat saber determinar l’acidesa relativa de diferents protons en les molècules és una de les habilitats més importants en química orgànica. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Introducció del Mètode A.R.I.O (MARIO) que permet determinar qualitativament l’acidesa de diferents hidrògens presents en una molècula. |
|
|
|
| |
Resum de Classe 1.03 |
|
|
|
| |
 |
|
|
|
| |
Classe: 1.04: Una introducció al mapa sintètic |
|
|
|
| |
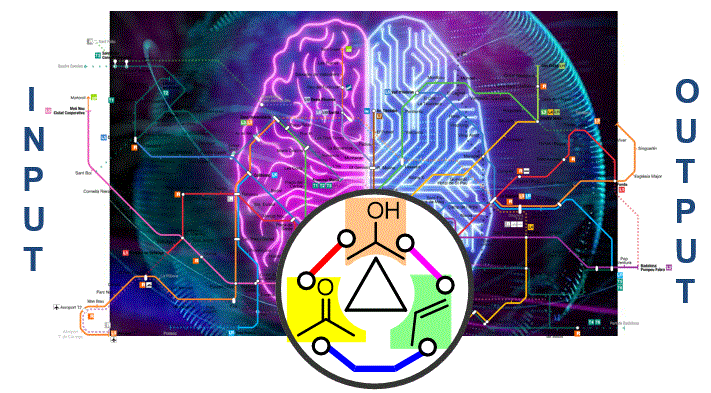
Les rutes sintètiques a molècules biològicament actives solen requerir múltiples passos en els quals transformem un grup funcional a un altre. Ser capaç d’organitzar el material mentalment i veure quines transformacions són possibles és una habilitat clau en la planificació de síntesis orgàniques. Si saps viatjar en metro, coneixes els conceptes bàsics sobre com planificar una ruta sintètica. |
|
|
|
| |
 |
|
|
|
| |
Resum de Classe 1.04 |
|
|
|
| |
Objectiu de Classe: Introducció del mapa sintètic, expliquem com s’organitza utilitzant conceptes basats en xarxes neuronals d'intel·ligència artificial. Explica com es pot utilitzar per planificar rutes sintètiques entre diferents grups funcionals. |
|
|
|
| |
 |
|
|
|
| |
Classe: 1.05: Una Introducció a Mecanismes |
|
|
|
| |
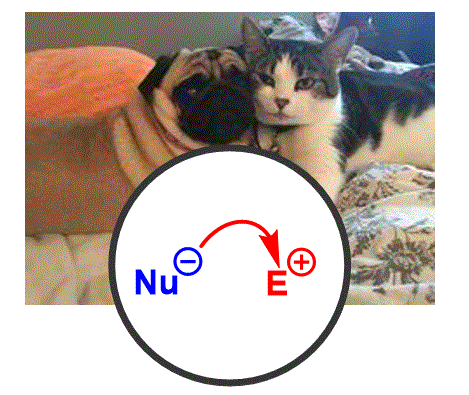
Les transformacions químiques es basen en algunes regles clau - l'atracció dels contraris. Comprendre aquestes regles fonamentals ens permet explicar com un grup funcional es transforma en un altre (mitjançant el mecanisme). |
|
|
|
| |
 |
|
|
|
| |
Resum de Classe 1.05 |
|
|
|
| |
Objectiu de Classe: S’introdueixen els conceptes de nucleòfil i electròfil i com reaccionen junts mitjançant fletxes corbes. S’explicaran les regles que regulen l’ús d’aquestes fletxes. |
|
|
|
| |
 |
|
|
|
| |
Classe 1.06: Mecanismes - Reactius Intermedis i Curs de la Reacció |
|
|
|
| |
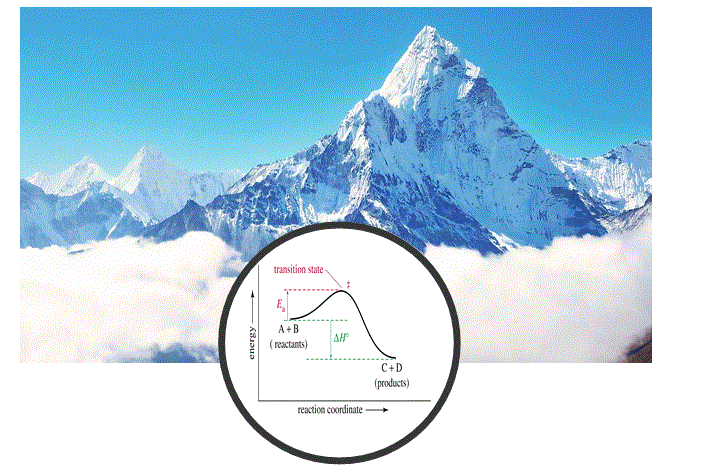
Quan les molècules reaccionen juntes, passen per estats intermedis d’alta energia inestables de curta durada a mesura que es trenquen i es formen els enllaços químics. Analitzant aquests intermedis podem determinar el mecanisme d’una reacció química. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Comprendre diversos aspectes sobre mecanismes com els intermedis formats (les seves estabilitats) i com podem representar una transformació sintètica en un diagrama energètic |
|
|
|
| |
Resum de Classe 1.06 |
|
|
|
| |
 |
|
|
|
| |
Classe: 1.07: Reaccions Radicalàries: Funcionalització d’alcans |
|
|
|
| |
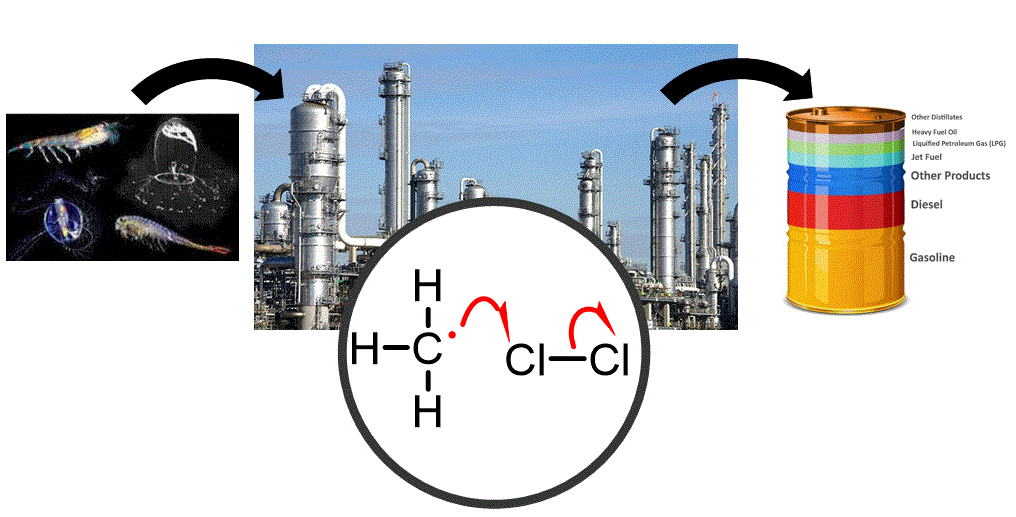
El nostre recorregut sintètic parteix dels alcans que són poc reactius i normalment s’utilitzen només com a combustibles o dissolvents. Tot i això, es poden transformar en molècules reactives (halurs d'alquil) mitjançant química radicalària. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Explicar com es poden transformar els alcans inerts en intermedis sintètics importants: clorurs d’alquil mitjançant reaccions radicalàries. |
|
|
|
| |
Resum de Classe 1.07 |
|
|
|
| |
Reaccions introduïdes: cloració radicalària d'alcans |
|
|
|
| |
 |
|
|
|
| |
Classe: 1.08: Selectivitat en Reaccions Radicalàries |
|
|
|
| |
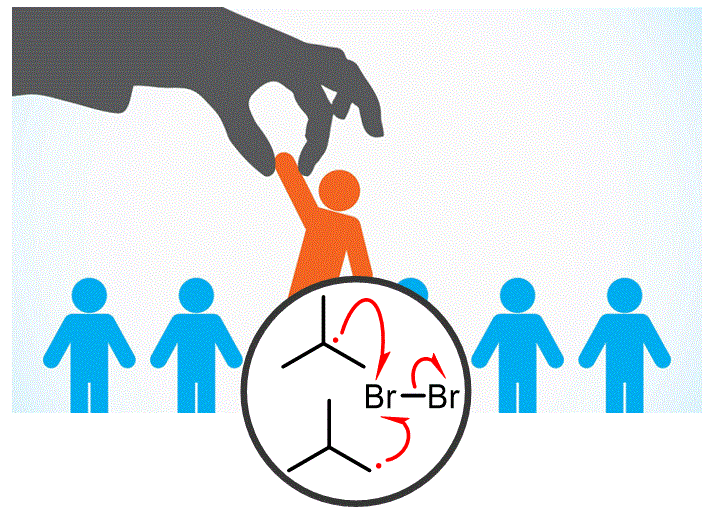
Un dels problemes de cloració d'alcans és que pot donar mescles amb alcans amb diferents tipus d'hidrògens. No obstant això, és possible obtenir selectivament un sol producte per bromació radicalària d'alcans. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Explicar com l’ús de diferents halògens en reaccions de substitució radicalària condueix a resultats diferents. Mostrar la major selectivitat obtinguda mitjançant la bromació. Com es pot utilitzar el reactiu NBS per afegir un àtom de brom en una posició al·lílica o benzíl·lica d’una molècula. |
|
|
|
| |
Resum de Classe 1.08 |
|
|
|
| |
Reaccions introduïdes: bromació d'alcans bromació al·lílica i benzíl·lica |
|
|
|
| |
 |
|
|
|
| |
TEMA 1.2: Reaccions de substitució nucleòfila alifàtica |
|
|
|
| |
 |
|
|
|
| |
Classe: 1.09: Reacció de substitució nucleòfila (SN2) |
|
|
|
| |
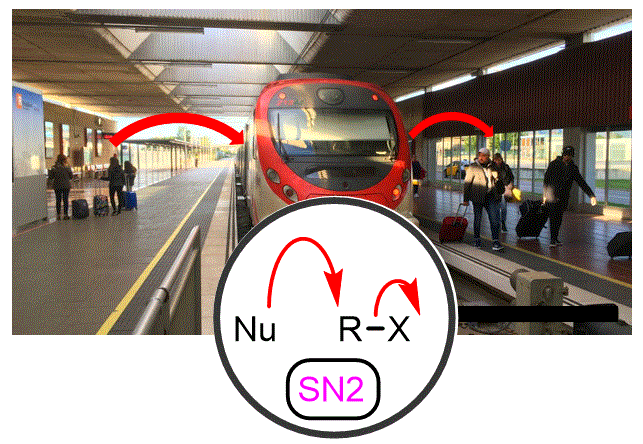
Els haloalcans que hem preparat en les dues classes anteriors es poden utilitzar com a materials de partida per sintetitzar una àmplia gamma de grups funcionals importants substituint l’halògen pel grup funcional d’interès. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Explicar el mecanisme per substituir l’halògen dels haloalcans per un altre àtom. S’introduiran quatre factors que ens ajudaran a determinar si la reacció serà favorable. |
|
|
|
| |
Resum de Classe 1.09 |
|
|
|
| |
Reaccions introduïdes:
Formació d’alcohols (SN2) Formació d’èters (SN2) Formació d’èsters (SN2) Formació de tiols (SN2) Formació de sulfurs (SN2) Formació de fosfines (SN2) Intercanvi d’halògens (SN2) (Finkelstein) Formació de nitrils (SN2) |
|
|
|
| |
 |
|
|
|
| |
Classe 1.10: Reacció de substitució nucleòfila (SN1) |
|
|
|
| |
Hi ha reaccions de substitució que funcionen mitjançant un mecanisme lleugerament diferent al que acabem d’estudiar i donaran diferents tipus de productes. Aquestes reaccions passen per un intermedi (un carbocatió). |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Introduïr la reacció SN1, utilitzar els mateixos quatre factors que hem estudiat anteriorment per explicar quins factors afavoreixen aquest mecanisme alternatiu. |
|
|
|
| |
Resum de Classe 1.10 |
|
|
|
| |
Reaccions introduïdes: Les mateixes reaccions que a la classe anterior però amb condicions diferents. |
|
|
|
| |
 |
|
|
|
| |
Classe 1.11 Substitució nucleòfila SN1 o SN2? |
|
|
|
| |
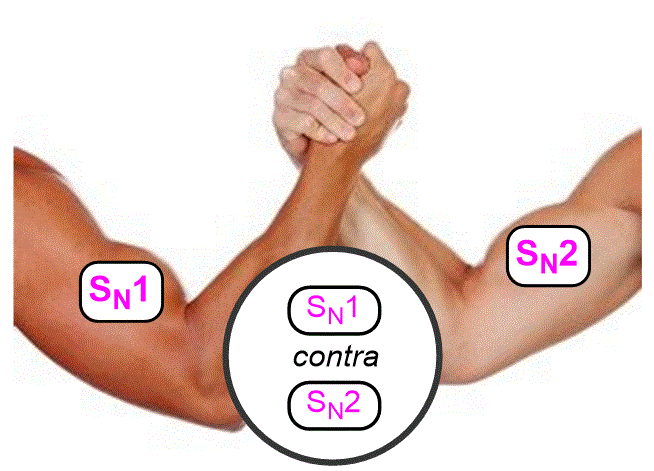
Hem discutit dos tipus de reaccions de substitució i els 4 factors que afavoreixen cada tipus de mecanisme. En molts casos pot ser difícil determinar quin factor guanyarà i, per tant, per quin mecanisme es produirà la reacció. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Farem una comparació directa de les 4 regles que hem utilitzat per determinar si una reacció SN1 o SN2 és favorable. Introduirem un procediment sistemàtic per veure quin mecanisme s’afavorirà. |
|
|
|
| |
Resum de Classe 1.11 |
|
|
|
| |
 |
|
|
|
| |
Classe: 1.12: Reaccions d’eliminació E2 |
|
|
|
| |
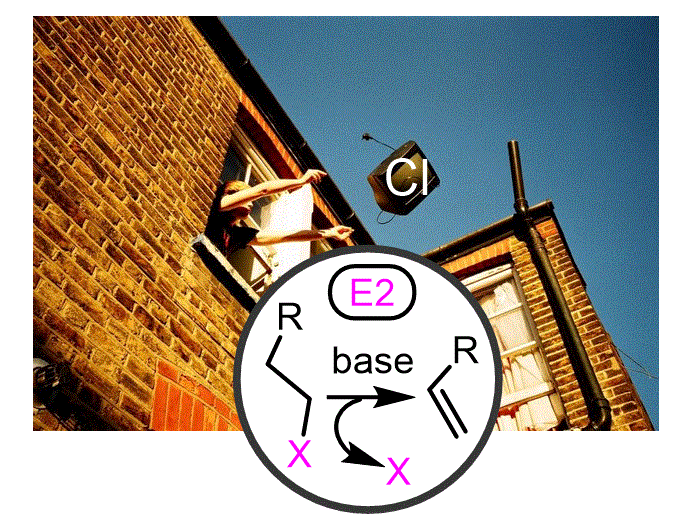
A les classes anteriors vam veure l’àtom d’halògen pot ser substituït per un altre àtom (el nucleòfil). Si l’halogenur d'alquil té un hidrogen present en posició beta és possible una altra tipus de reacció: l’eliminació. Aquest procés condueix a l'eliminació de l'halògen i un hidrogen i la formació d’un alquè. Aquest procés ens permet ampliar les nostres possibilitats sintètiques. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Explicar el mecanisme de com s'eliminen els substituents per donar alquens. Definir els requisits necessaris perquè la reacció tingui lloc. |
|
|
|
| |
Resum de Classe 1.12 |
|
|
|
| |
Reaccions introduïdes: Eliminació [E2] Base forta impedida |
|
|
|
| |
 |
|
|
|
| |
Classe: 1.13: Reaccions d’eliminació E1 |
|
|
|
| |
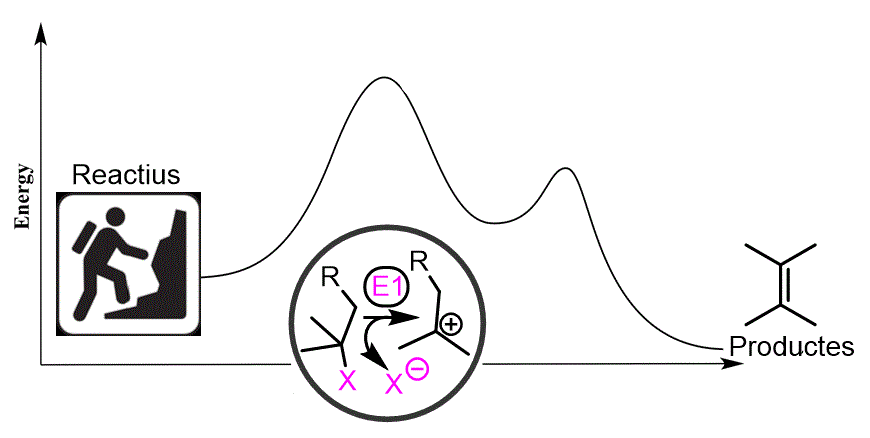
De la mateixa manera que hi ha dos tipus de reaccions de substitució, hi ha dos tipus de reaccions d'eliminació: el concertat (E2) i el no concertat (E1). La reacció d'eliminació de l'E1 (igual que l'SN1) passa a través d'un intermedi de carbocatió. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: |
|
|
|
| |
Resum de Classe 1.13 |
|
|
|
| |
Reaccions introduïdes: Eliminació [E1] de ROH |
|
|
|
| |
 |
|
|
|
| |
Classe: 1.14: Reaccions d’Eliminació vs Substitució |
|
|
|
| |
Fins ara hem vist que els haloalcans poden experimentar reaccions de substitució (SN1 o SN2) o reaccions d’eliminació (E1 o E2). Quin mecanisme dominarà? Intentar determinar-ho pot ser un maldecap! |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Introduïr un enfocament sistemàtic que ens ajudi a determinar quin procés estarà en funcionament en funció del substrat, el grup sortint, el nucleòfil (o base) i el dissolvent. |
|
|
|
| |
Resum de Classe 1.14 |
|
|
|
| |
Reaccions introduïdes: Cap - aquesta classes actuarà com un resum. |
|
|
|
| |
 |
|
|
|
| |
 |
|
|
|
| |
Al bloc 2 ens movem de zona del mapa sintètic per discutir les reaccions dels sistemes C = C sp2 (alquens, alquins i anells aromàtics). |
|
|
|
| |
 |
|
|
|
| |
TEMA 2.1: Reaccions dels hidrocarburs insaturats |
|
|
|
| |
 |
|
|
|
| |
Classe: 2.01: Alquens: reaccions d’addició: Introducció General |
|
|
|
| |
Una reacció important dels alquens és el que s’anomena reacció d’addició on el reactiu s’afegeix a sobre del doble enllaç. Si l’alquè no és simètric, el reactiu (X-Y) es pot orientar de dues maneres possibles i conduir a productes diferents. Per descriure quina orientació donen els reactius, necessitem un sistema de nomenclatura per descriure aquest procés. Afortunadament, Vladímir Markóvnikov ens va proporcionar un sistema d’aquest tipus. |
|
|
|
| |
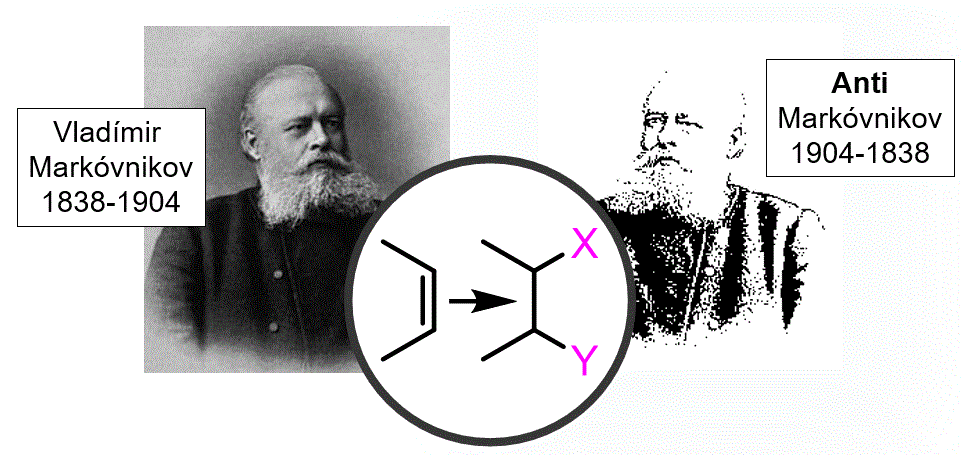 |
|
|
|
| |
Objectiu de Classe: Introduïr un sistema de nomenclatura que ens permeti descriure com s'ha afegit un substituent a un alquè. |
|
|
|
| |
Resum de Classe 2.01 |
|
|
|
| |
Reaccions introduïdes: cap |
|
|
|
| |
 |
|
|
|
| |
Classe: 2.02: Alquens: Addició de 2 grups diferents: H + X |
|
|
|
| |
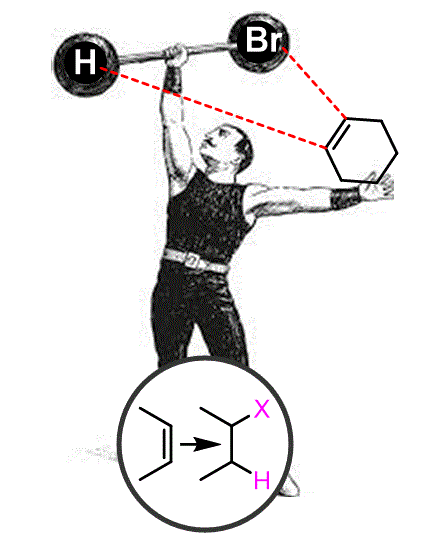
Fins ara hem discutit com formar haloalcans afegint halògens als alcans. També podem obtenir haloalcans per addició d’àcids com HCl i HBr als alquens. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Explicar el mecanisme per a l’addició d’àcids als alquens amb selectivitat de Markovnikov o anti-Markovnikov. |
|
|
|
| |
Resum de Classe 2.02 |
|
|
|
| |
Reaccions introduïdes: Addició de HX (HCl, HBr) a alquens Addició radicalària de HBr |
|
|
|
| |
 |
|
|
|
| |
Classe: 2.03: Alquens: Addició de 2 grups diferents: H + OH |
|
|
|
| |
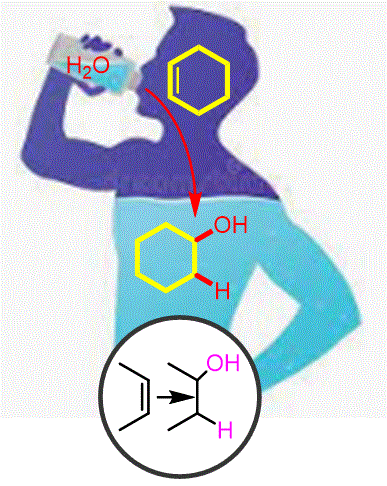
L’addició d’aigua a través d’un doble enllaç (hidratació) és una estratègia important per accedir al grup funcional de l’alcohol. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Explica com podem afegir H + OH a través d’un doble enllaç amb selectivitat de Markovnikov o anti-Markovnikov. |
|
|
|
| |
Resum de Classe 2.03 |
|
|
|
| |
Reaccions introduïdes: Hidratació d’alquens Hidroboració |
|
|
|
| |
 |
|
|
|
| |
Classe: 2.04: Alquens: reaccions d’addició de 2 grups iguals: H, Br o O |
|
|
|
| |
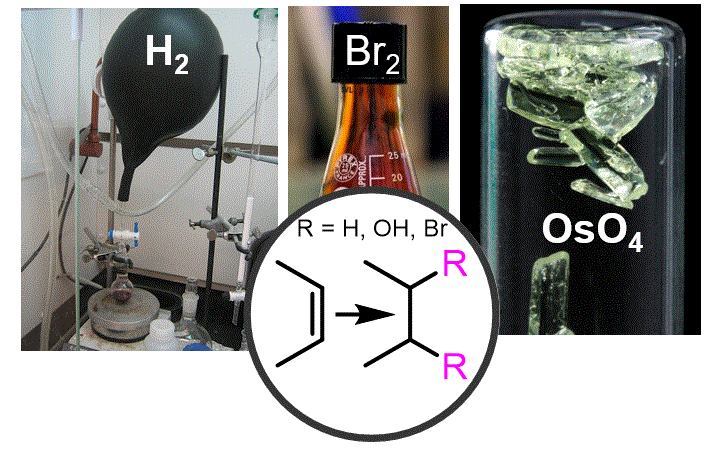
Fins ara hem afegit 2 grups diferents sobre alquens, ja sigui H + X o H + OH amb un enfocament en la selectivitat de Markovnikov o anti-Markovnikov. Quan els dos àtoms són iguals, aquests problemes de selectivitat es tornen irrellevants. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Expliqueu com afegir 2 hidrògens, 2 broms o 2 alcohols a sobre d’un doble enllaç. |
|
|
|
| |
Resum de Classe 2.04 |
|
|
|
| |
Reaccions introduïdes: Hidrogenació d’alquens Addició d’halògen Dihidroxilació d’alquens |
|
|
|
| |
 |
|
|
|
| |
Classe: 2.05: Epòxids: Intermedis clau en la síntesi |
|
|
|
| |
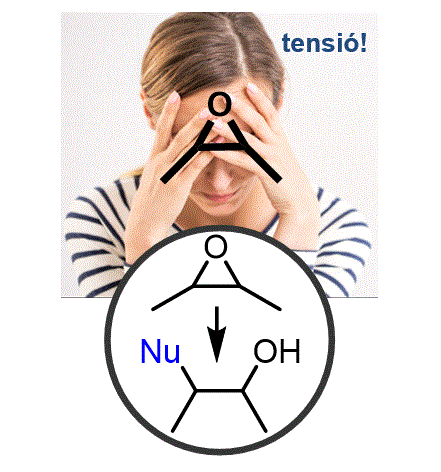
Els epòxids són anells amb molta tensió que volen obrir-se per alleujar l'alta tensió de l'anell. Podem aprofitar aquesta tendència utilitzant-los com a electròfils molt reactius que en obrir-se donen accés a alcohols. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Explicar com formar epòxids, la reactivitat dels epòxids amb diversos nucleòfils i com podem obrir selectivament epòxids no simètrics. |
|
|
|
| |
Resum de Classe 2.05 |
|
|
|
| |
Reaccions introduïdes: Formació d’epòxids d’halohidrines Formació d’halohidrines Epoxidació Obertura d’epòxids amb Nu |
|
|
|
| |
 |
|
|
|
| |
Classe: 2.06: Reaccions dels alquins |
|
|
|
| |
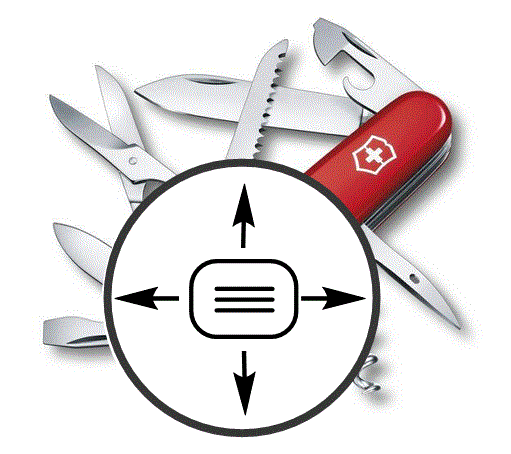
Els alquins no són grups funcionals molt comuns en productes farmacèutics i naturals. Tot i això, són productes intermedis sintètics molt versàtils. Són nucleòfils ideals per fer enllaços carboni-carboni i el triple enllaç dels productes resultants es pot reduir selectivament per donar alquens E o Z. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Introduïr les reaccions importants dels alquins que il·lustren la seva gran utilitat. |
|
|
|
| |
Resum de Classe 2.06 |
|
|
|
| |
Reaccions introduïdes: Desprotonació d’alquins Ions d’acetilur Alquilació Ions d’acetilur Obertura d'epòxids Reducció Lindlar Hidrogenació parcial d‘alquins Hidrogenació d’alquins Conversió de 1,2 dihaloalcans a alquins Hidratació de alquins |
|
|
|
| |
 |
|
|
|
| |
Classe: 2.07: Reaccions dels diens conjugats |
|
|
|
| |
La reacció de Diels-Alder és una de les reaccions més importants i útils en química sintètica que permet sintetitzar sistemes d’anells de 6 membres presents en molts compostos importants. El mecanisme representa una nova classe de reaccions, les reaccions pericícliques. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Introducció de la reacció de Diels Alder, els requisits dels materials de partida perquè es produeixi la reacció. |
|
|
|
| |
Resum de Classe 2.07 |
|
|
|
| |
Reaccions introduïdes: Reacció de Diels-Alder |
|
|
|
| |
 |
|
|
|
| |
TEMA 2.2: Reaccions del benzè i dels seus derivats |
|
|
|
| |
 |
|
|
|
| |
Classe: 2.08: Substitució electròfila aromàtica |
|
|
|
| |
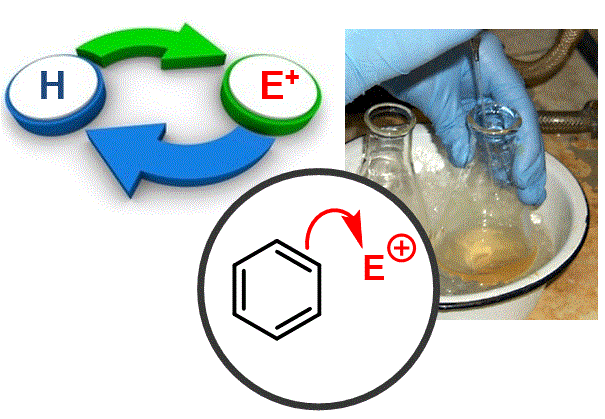
Vam veure a la classe 2.04 que era possible afegir un electròfil (com el brom) a un alquè. Tot i que els compostos aromàtics són semblants als alquens, l'estabilitat de l'anell aromàtic canvia significativament la seva química: ara hem d'activar l'electròfil (amb un àcid de Lewis o un àcid de Brönsted). A més, en lloc d'una reacció d'addició obtenim una substitució per tal de regenerar el sistema aromàtic. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Introduir el concepte de substitució aromàtica d'electròfils mitjançant les reaccions de bromació i nitració. |
|
|
|
| |
Resum de Classe 2.08 |
|
|
|
| |
Reaccions introduïdes: Halogenació aromàtica, Nitració aromàtica |
|
|
|
| |
 |
|
|
|
| |
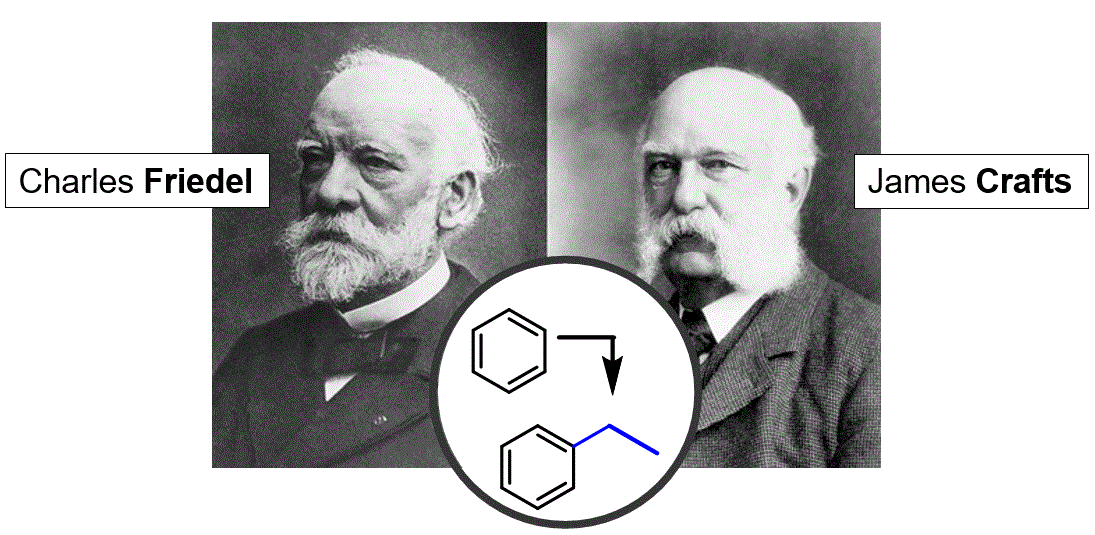
Classe: 2.09: Substitució electròfila aromàtica – Reacció de Friedel Crafts: alquilació i acilació |
|
|
|
| |
Si volem unir àtoms de carboni a un anell de benzè, utilitzem una estratègia similar a la introduïda a la classe anterior: generem un electròfil de carboni activat (utilitzant un àcid de Lewis) per reaccionar amb l'anell de benzè (el nucleòfil). Aquest procés és un dels més importants de la química orgànica i va ser descobert per Friedel i Crafts. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Explicar com introduir cadenes de carboni als anells aromàtics mitjançant la reacció d'alquilació de Friedel-Crafts. Explicar quan poden sorgir complicacions i com evitar aquest problema mitjançant un enfocament de 2 passos: Acilació de Friedel-Crafts i reducció de Clemmensen. |
|
|
|
| |
Resum de Classe 2.09 |
|
|
|
| |
Reaccions introduïdes: Alquilació de Friedel-Crafts,
Acilació Friedel-Crafts, Reducció de Clemmensen |
|
|
|
| |
 |
|
|
|
| |
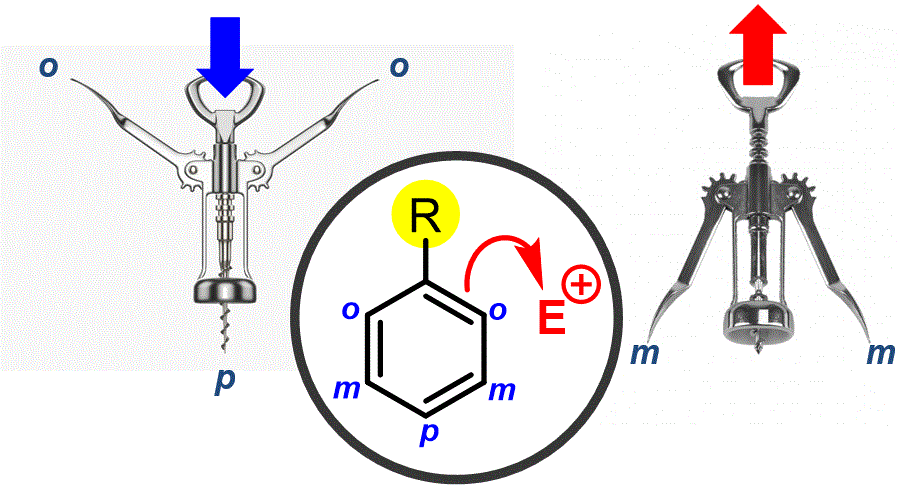
Classe: 2.10: Substitució Electròfila Aromàtica en benzens mono-substituïts. |
|
|
|
| |
Podem modificar la reactivitat de l'anell de benzè en funció dels substituents presents. Si l'anell té un grup donant és més ric en electrons i, per tant, més nucleòfil (més reactiu). D'altra banda, els grups que treuen electrons fan que l'anell sigui pobre en electrons i, per tant, menys nucleòfil (menys reactiu). Aquests grups també influiran molt la posició de substitució de l'electròfil introduït. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Discutir els efectes dels substituents sobre l'anell de benzè en el resultat de les reaccions de substitució d'electròfils aromàtics. Mirar l'efecte de cada substituent de manera sistemàtica per determinar-ne els efectes directius. |
|
|
|
| |
Resum de Classe 2.10 |
|
|
|
| |
Reaccions introduïdes: cap |
|
|
|
| |
 |
|
|
|
| |
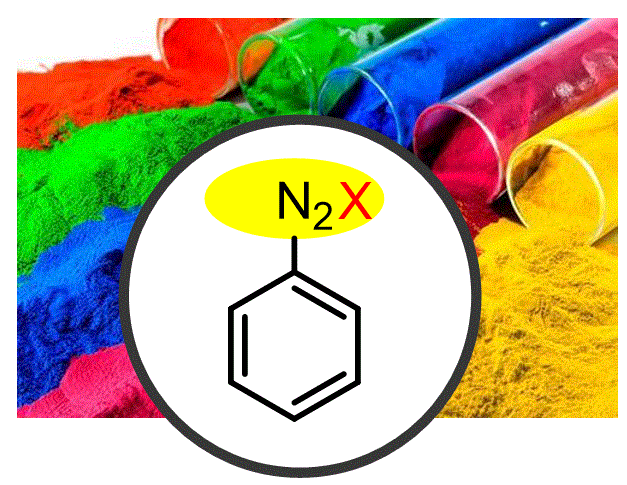
Classe: 2.11: Sals d’arildiazoni com a intermediaris de síntesi: |
|
|
|
| |
Els compostos diazo són intermedis reactius importants que ens permeten introduir selectivament substituents a l'anell aromàtic. A més, aquests compostos són intermedis importants per a la síntesi de colorants i productes farmacèutics. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Explicar com es formen els compostos diazoics a partir de compostos nitro i anilines i com es poden utilitzar en la síntesi. |
|
|
|
| |
Resum de Classe 2.11 |
|
|
|
| |
Reaccions introduïdes: Formació de diazocompostos, Reacció de Sandemeyer, Reacció de Shiemann, Acoblament Diazo. |
|
|
|
| |
 |
|
|
|
| |
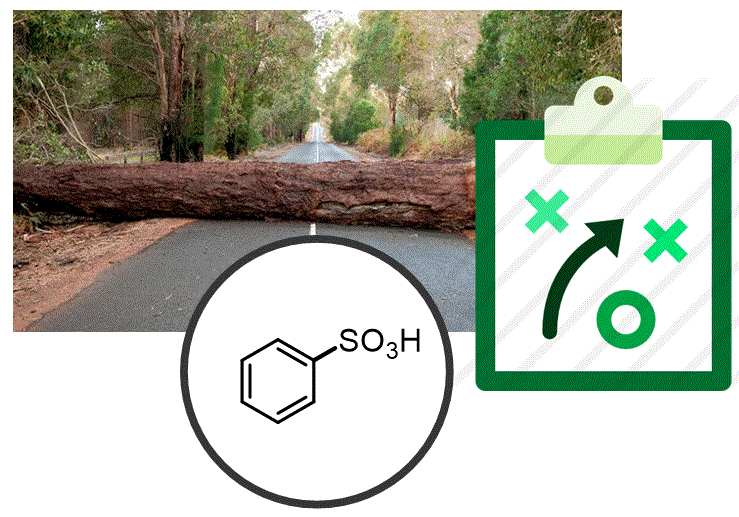
Classe: 2.12: Sulfonació i Estratègies en Substitució Electròfila Aromàtica |
|
|
|
| |
L'addició del grup sulfonil a un anell aromàtic és un procés reversible. És possible utilitzar aquest grup per bloquejar temporalment determinades posicions de l'anell aromàtic per evitar reaccions no desitjades en aquestes posicions. Un cop hem introduït el nostre substitut en la posició correcta podem eliminar el grup sulfonil. A més, el grup sulfonil i els seus derivats es troben en molts compostos farmacèutics importants. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Mostrar com utilitzar el grup sulfonil en estratègies sintètiques per introduir selectivament substituents a la posició desitjada. |
|
|
|
| |
Resum de Classe 2.12 |
|
|
|
| |
Reaccions introduïdes: Sulfonació aromàtica, Preparació de benzensulfonils, Desprotonació d’àcids benzensulfònics, Síntesi de sulfonamides |
|
|
|
| |
 |
|
|
|
| |
Classe: 2.13: Substitució nucleòfila aromàtica del benzè i els seus derivats. |
|
|
|
| |
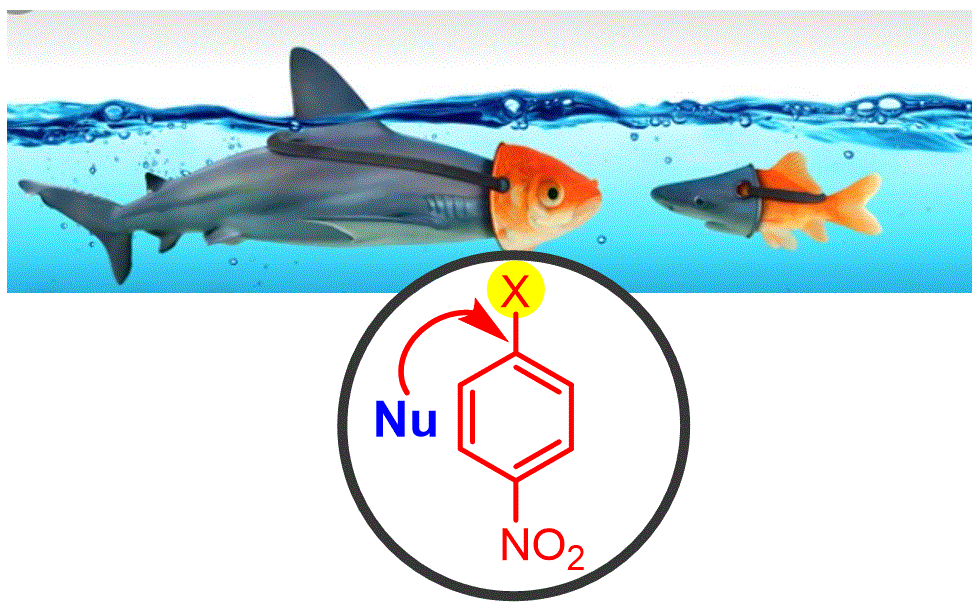
Fins ara hem parlat de les reaccions de substitució electròfila aromàtica dels anells de benzè (SEAR). En totes aquestes reaccions l'anell de benzè actua com a nucleòfil i reacciona amb diversos electròfils. En aquesta classe ens preguntem "podem canviar el paper de l'anell de benzè i utilitzar-lo com a electròfil i atacar-lo amb una sèrie de nucleòfils?" La resposta és "sí", però cal que hi hagi certs criteris importants perquè la reacció funcioni. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Mostrar com fem servir els anells de benzè com a electròfils en un nou tipus de reacció: la substitució nucleòfila aromàtica (SNAR). Discutiu els requisits especials que s'han de complir perquè aquesta reacció funcioni. |
|
|
|
| |
Resum de Classe 2.13 |
|
|
|
| |
Reaccions introduïdes: Substitució Nucleòfila Aromàtica, Fusió amb NaOH |
|
|
|
| |
 |
|
|
|
| |
TEMA 2.3. Heterocicles aromàtics |
|
|
|
| |
 |
|
|
|
| |
Classe: 2.14: Heterocicles Aromàtics: Una Introducció |
|
|
|
| |
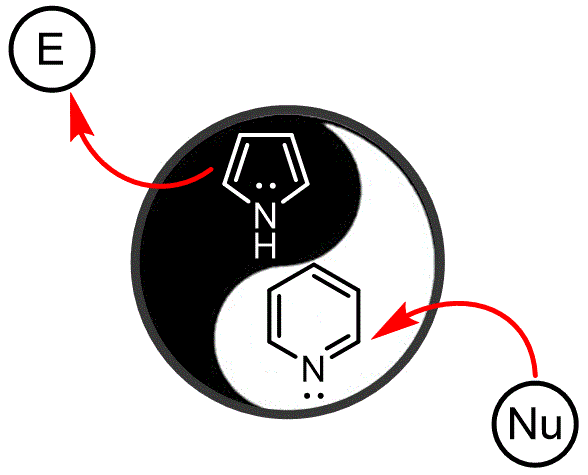
Els compostos heterocíclics es troben en molts compostos farmacèutics. Tot i que la química dels heterocicles és àmplia i requereix un curs propi, en aquest curs introductori donem una visió general dels punts més importants. Ens centrem en 2 dels heterocicles més importants: els anells de pirrol i piridina que presenten propietats polars oposades. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: En aquesta classe introductòria es discuteixen els efectes dels diferents components que constitueixen les diferents estructures heterocícliques i introduïm 4 regles claus que ens permeten entendre la reactivitat i les propietats d'aquests sistemes d'anells. |
|
|
|
| |
Resum de Classe 2.14 |
|
|
|
| |
 |
|
|
|
| |
Classe: 2.15: Heterocicles Aromàtics pi-deficients |
|
|
|
| |
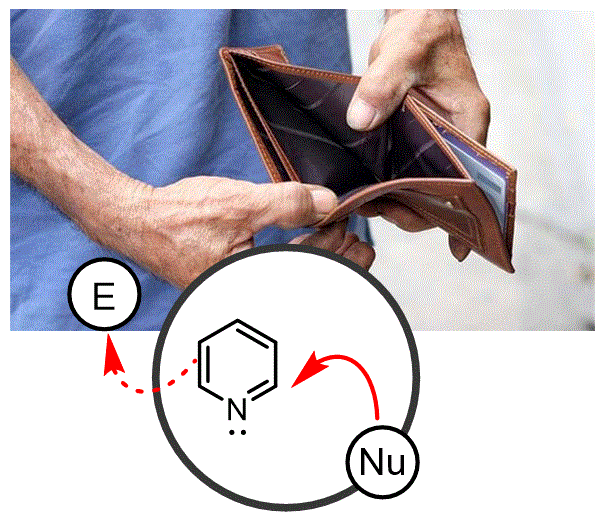
En aquesta classe analitzem amb més detall els heterocicles que contenen nitrogen de 6 membres (piridines) i els seus derivats. Aquests sistemes d'anells són pobres en electrons i tenen un nitrogen bàsic. Això fa que tinguin l'efecte de fer-los millors electròfils que nucleòfils en les reaccions de substitució aromàtica. La presència del nitrogen els fa bàsics, una propietat que també disminueix la seva capacitat de patir reaccions de substitució electròfila. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Discutir l'estructura de la piridina i els seus derivats i les reaccions clau que experimenten aquests compostos. |
|
|
|
| |
Resum de Classe 2.15 |
|
|
|
| |
Reaccions introduïdes: reacció de Chichibabin, |
|
|
|
| |
 |
|
|
|
| |
Classe: 2.16: Heterocicles pi-excedents |
|
|
|
| |
Els heterocicles de cinc membres (pirrol, furà i tiofè) són molt rics en electrons, cosa que els fa reaccionar només com a nucleòfils en reaccions de substitució d'electròfils aromàtics. Són tan rics en electrons que veurem que moltes reaccions SEAR tenen lloc en condicions molt més suaus que amb els anells de benzè. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Discutir l'estructura dels heterocicles de 5 membres i les seves reaccions clau. Explicar l'efecte d'afegir grups de piridina tipus C=N (imidazole) i anells aromàtics fusionats (indole) i com això afecta la reactivitat de l'estructura matriu (pirrole). |
|
|
|
| |
Resum de Classe 2.16 |
|
|
|
| |
Reaccions introduïdes: variacions de les reaccions que hem vist per als anells de benzè |
|
|
|
| |
 |
|
|
|
| |
 |
|
|
|
| |
Al bloc 3 ens movem a la zona dels carbonils per discutir les reaccions dels sistemes C = O (sp2). |
|
|
|
| |
 |
|
|
|
| |
TEMA 3.1. Aldehids i cetones. Reaccions d'addició nucleòfila |
|
|
|
| |
 |
|
|
|
| |
Classe: 3.01: Formació de compostos carbonílics mitjançant oxidació |
|
|
|
| |
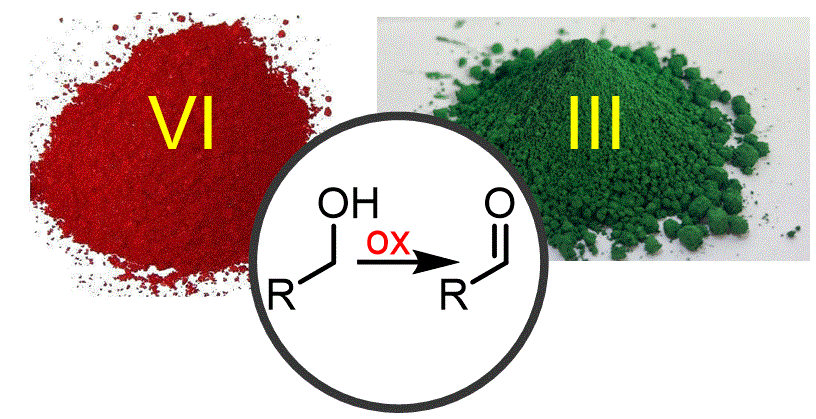
La reactivitat dels compostos carbonílics representa una àrea important de la química orgànica. Comencem aquesta secció del curs discutint les maneres clau de sintetitzar compostos carbonílics a partir d'alcohols. |
|
|
|
| |
 |
|
|
|
| |
|
|
|
|
| |
Objectiu de Classe: Mostrar com es poden formar aldehids, cetones i àcids carboxílics a partir d'alcohols mitjançant el procés d'oxidació. Discutir quins reactius hem d'utilitzar per obtenir selectivament un aldehid o un àcid quan s'utilitza un alcohol primari com a substrat. |
|
|
|
| |
Resum de Classe 3.01 |
|
|
|
| |
Reaccions introduïdes: Oxidació de PCC, Oxidació de PDC, Oxidació de Jones, Ozonòlisi |
|
|
|
| |
 |
|
|
|
| |
Classe: 3.02: |
|
|
|
| |
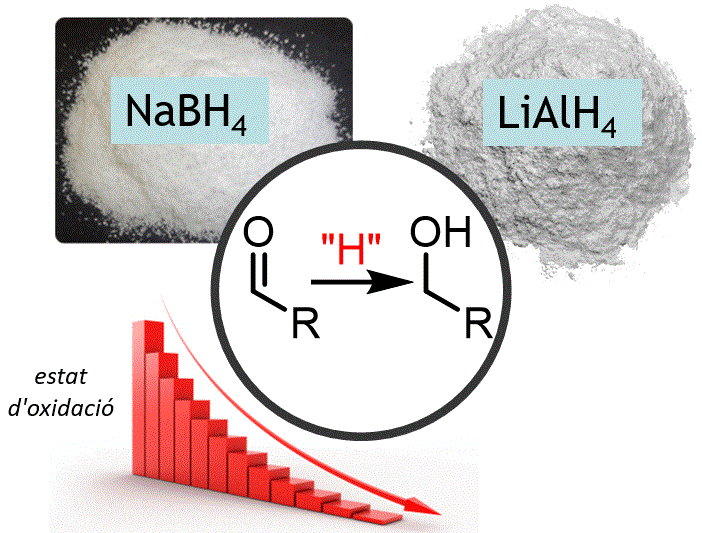
A la classe anterior vam comentar com oxidar els alcohols a aldehids, cetones i àcids carboxílics. En aquesta classe parlem del procés invers: com reduir els compostos carbonílics a alcohols. |
|
|
|
| |
 |
|
|
|
| |
|
|
|
|
| |
Objectiu de Classe: Mostrar com reduir els compostos carbonílics a alcohols utilitzant 2 reactius important: NaBH4 i LiAlH4 |
|
|
|
| |
Resum de Classe 3.02 |
|
|
|
| |
Reaccions introduïdes: Reducció amb NaBH4, Reducció amb LiAlH4 |
|
|
|
| |
 |
|
|
|
| |
Classe: 3.03: Addició nucleòfila d’alcohols i tiols |
|
|
|
| |
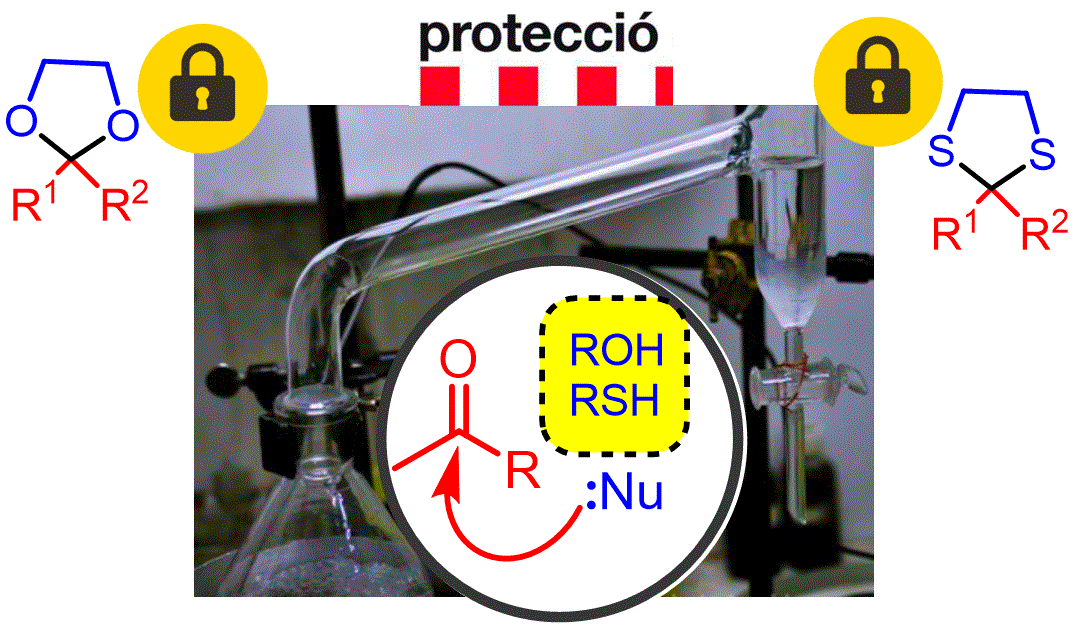
Hem vist a la classe anterior que els compostos carbonílics són atacats per H- (hidrur) per donar alcohols. En aquesta classe observem l'addició al grup carbonílic d'alcohols (per donar acetals) i tiols (per donar tioacetals). Com que aquest procés és reversible, podem utilitzar aquests compostos com a grups protectors del carbonil mentre realitzem altres reaccions sobre la resta de la molècula (i evitar reaccions no desitjades). |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Mostrar com reaccionen les cetones amb els alcohols per donar acetals. Discutir quins factors poden afavorir la reacció i com podem manipular la posició d'equilibri. També es parlarà breument dels compostos de sofre relacionats (tioacetals) i com podem utilitzar aquest grup per eliminar el grup carbonil. |
|
|
|
| |
Resum de Classe 3.03 |
|
|
|
| |
Reaccions introduïdes: Formació d'acetals, desprotecció d'acetals, formació de tioacetals, desprotecció de tioacetal, eliminacío de tioacetals amb Níquel Raney. |
|
|
|
| |
 |
|
|
|
| |
Classe: 3.04: Addició nucleòfila d’amines |
|
|
|
| |
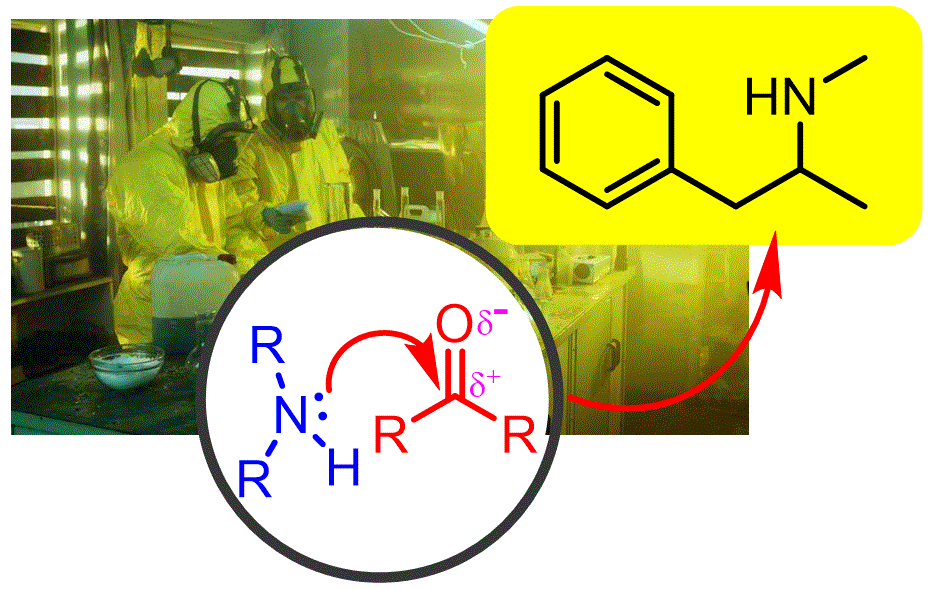
El nitrogen es troba habitualment en productes farmacèutics. En aquesta classe veurem com afegim amines (el nucleòfil) als aldehids i cetones (l'electròfil) per sintetitzar amines més complexes. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Mostrar com les amines reaccionen amb aldehids i cetones per formar imines o enamines segons el tipus d'amina emprada. Discutiu l'addició d'altres compostos nitrogenats (hidroxilamines, hidrazines). Mostrar com la reducció d'aquests compostos pot donar amines complexes o com podem utilitzar el grup per eliminar el carbonil (mitjaçant hidrazones). |
|
|
|
| |
Resum de Classe 3.04 |
|
|
|
| |
Reaccions introduïdes: Formació de imines, Formació de enamines, Aminació reductiva, Reducció de Wolf-Kishner |
|
|
|
| |
 |
|
|
|
| |
Classe: 3.05: Addició nucleòfila de carboni |
|
|
|
| |
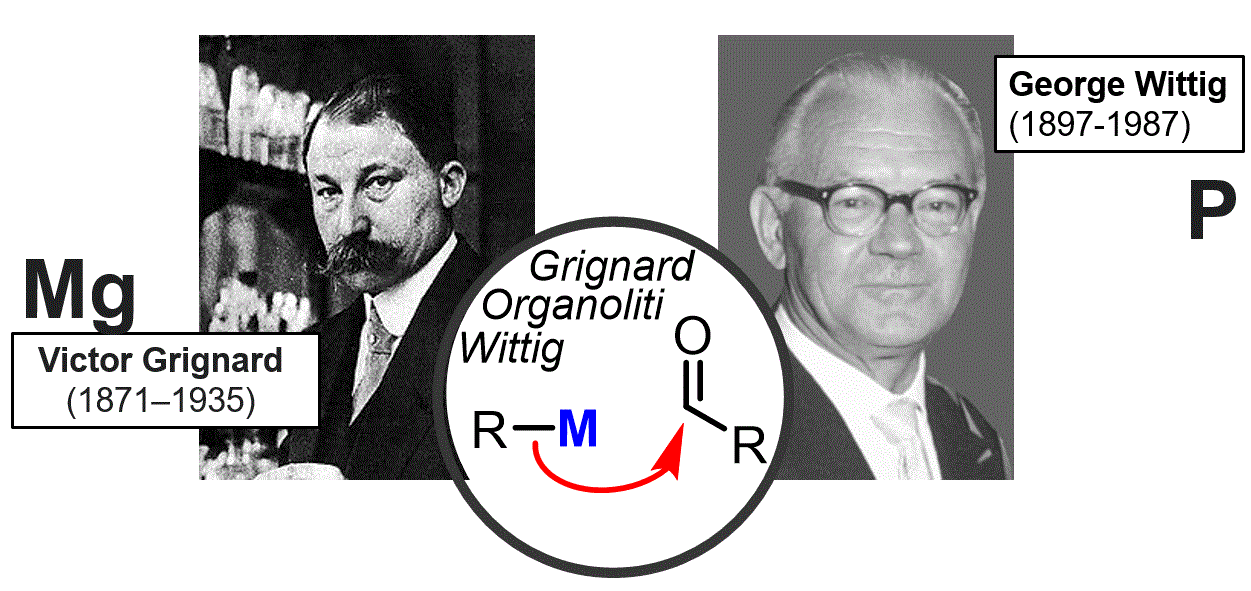
Per completar aquesta secció parlem de l'addició de nucleòfils de carboni als aldehids o cetones. Quan combinem l'àtom de carboni amb el magnesi (el reactiu de Grignard) o amb el fòsfor (el reactiu de Wittig) podem formar importants nucleòfils de carboni que podem afegir als aldehids o cetones. Aquestes reaccions representen 2 de les reaccions de formació d'enllaços C-C més potents de la química orgànica. |
|
|
|
| |
 |
|
|
|
| |
|
|
|
|
| |
Objectiu de Classe: Mostrar com s'afegeixen reactius de Grignard als carbonis per formar alcohols. Mostrar com s'afegeix el reactiu de Wittig al grup carbonil per formar alquens. |
|
|
|
| |
Resum de Classe 3.05 |
|
|
|
| |
Reaccions introduïdes: Addició de Grignard, Reacció de Wittig |
|
|
|
| |
 |
|
|
|
| |
TEMA 3.2: Àcids carboxílics i els seus derivats. Reaccions de substitució en el grup acil |
|
|
|
| |
 |
|
|
|
| |
Classe: 3.06: Àcids carboxílics i formació del seus derivats. |
|
|
|
| |
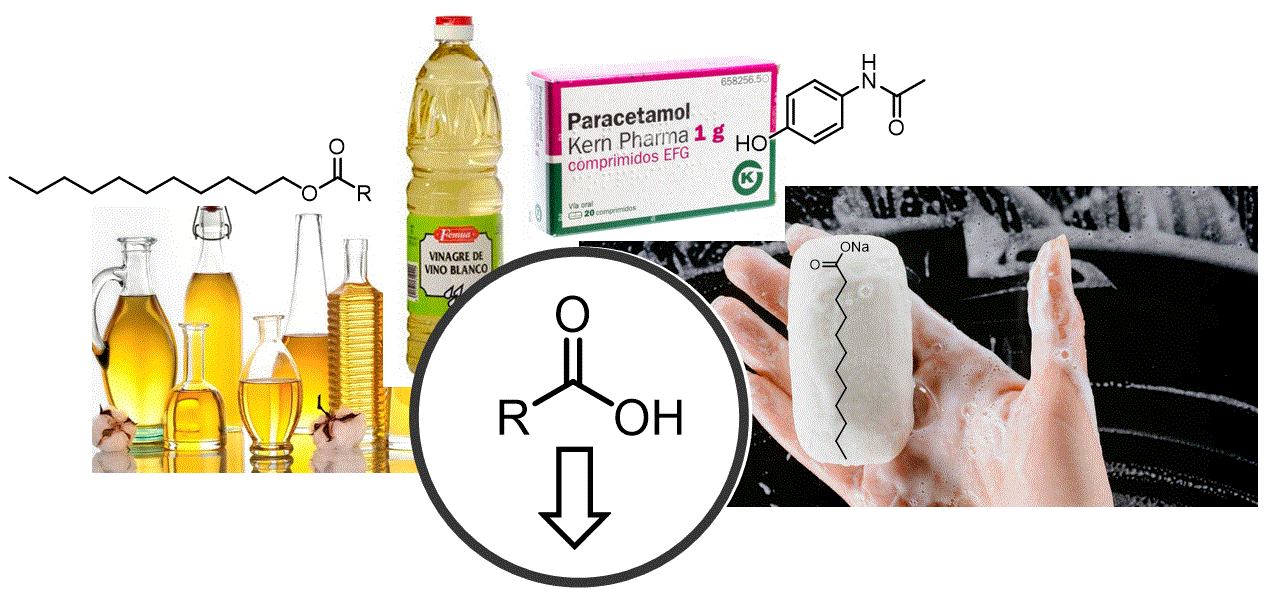
Passem ara a estudiar els compostos carbonílics amb un estat d'oxidació més alt (nivell 3). Els àcids carboxílics es poden considerar el compost mare a partir del qual es poden formar tots els altres compostos relacionats. Intercanviant el grup OH per NR2 (amides), OR (èsters), Cl (clorurs d'àcid) o RCO2 (anhídrids). |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Mostrar com es poden fer tots els altres compostos carbonílics relacionats amb un estat d'oxidació 3 mitjançant un nou concepte mecanístic: les reaccions d'eliminació d'addició nucleòfila. |
|
|
|
| |
Resum de Classe 3.06 |
|
|
|
| |
Reaccions introduïdes: Formació de clorurs d'àcid amb SOCl2, Formació d'èsters a partir de clorurs d'àcid |
|
|
|
| |
 |
|
|
|
| |
Classe: 3.07: Reaccions dels derivats dels àcids carboxílics: Èsters i Amides |
|
|
|
| |
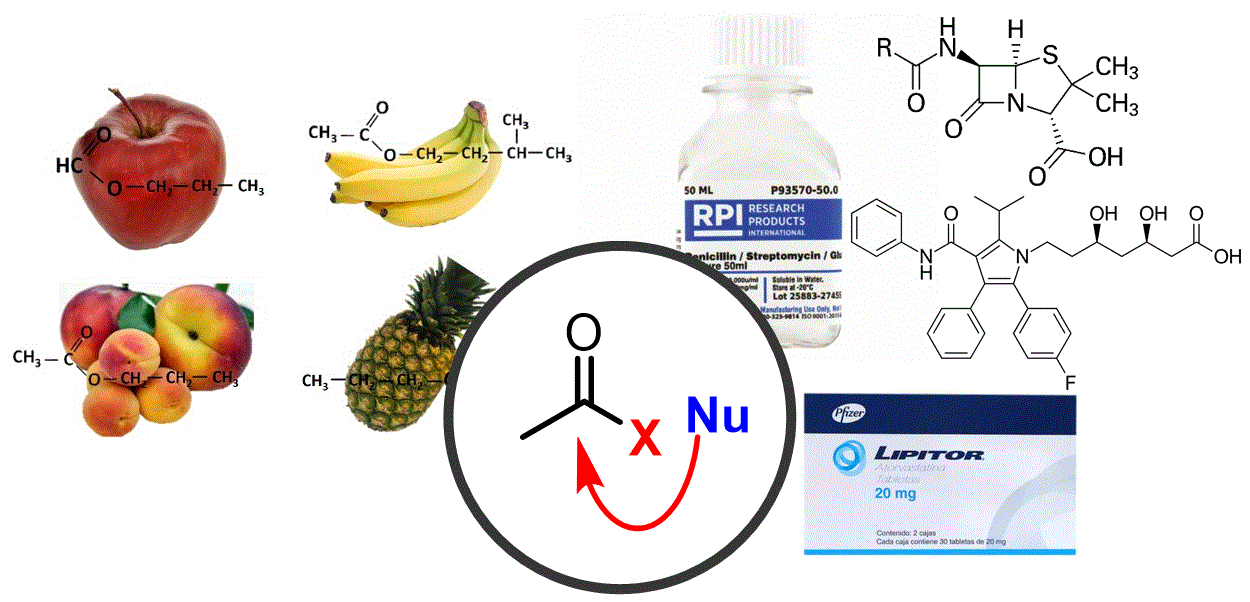
En aquesta classe desenvolupem encara més la química dels derivats d'àcids carboxílics centrant-nos en les reaccions d'èsters i amides. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Discutir com formar èsters i amides a partir d'àcids carboxílics, així com convertir-los de nou en àcid mitjançant la hidròlisi. |
|
|
|
| |
Resum de Classe 3.07 |
|
|
|
| |
Reaccions introduïdes: Esterificació de Fischer, Hidròlisi d’èsters (Saponificació), Transesterificació, Hidròlisi d’amides catalitzada per àcid |
|
|
|
| |
 |
|
|
|
| |
TEMA 3.3: Compostos carbonílics. Reaccions sobre la posició alfa i
reaccions de condensació |
|
|
|
| |
 |
|
|
|
| |
Classe: 3.08: Aldehids i cetones: Reaccions a la posició alfa: Introducció |
|
|
|
| |
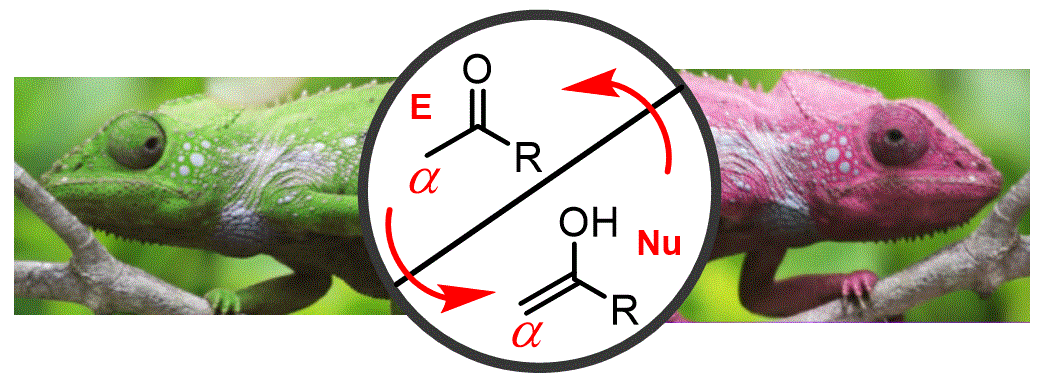
Fins ara hem vist que el grup carbonil actua com a electròfil i és atacat per una àmplia gamma de grups funcionals. En aquesta classe veurem com utilitzar-lo com a nucleòfil mitjançant enols i enolats. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Mostrar com identificar protons alfa en grups carbonil, discutir la formació d'enols i enolats i introduir reaccions de bromació en alfa que introdueixen el carbonil com a nucleòfil. |
|
|
|
| |
Resum de Classe 3.08 |
|
|
|
| |
Reaccions introduïdes: Halogenació d’enols, Reacció de Hell-Volhard-Zelinsky |
|
|
|
| |
 |
|
|
|
| |
Classe: 3.09: Aldehids i cetones:Reaccions a la posició alfa: enllaços C-C |
|
|
|
| |
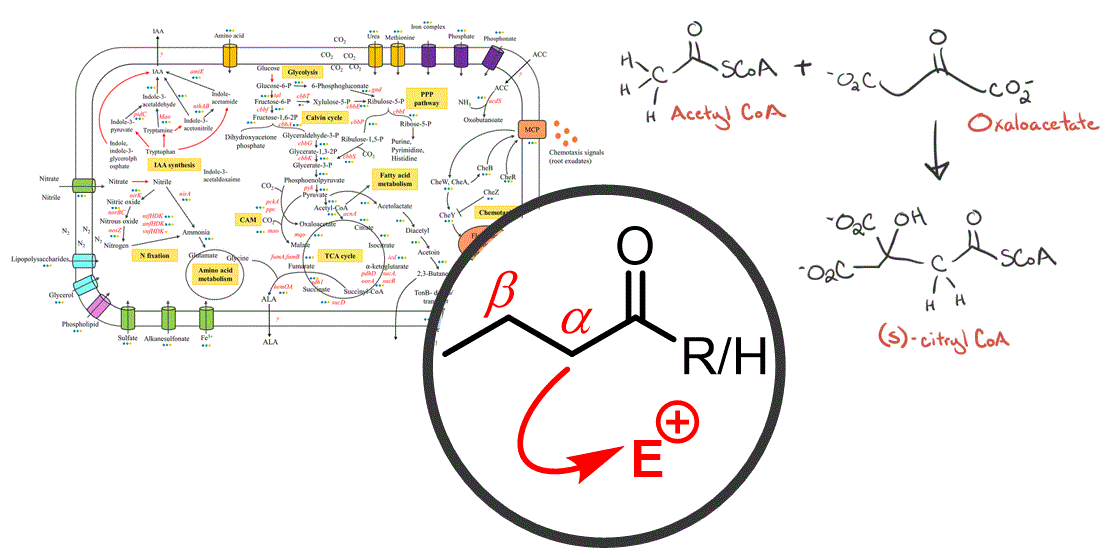
Fins ara hem vist que els compostos carbonílics poden actuar com a nucleòfils i electròfils. Per tant, és possible tenir reaccions entre compostos carbonílics on una molècula amb carbonil actua com a nucleòfil i una altra molècula amb carbonil actua com a electròfil. Aquestes reaccions de condensació no només són útils sintèticament al laboratori, sinó que també formen la base de molts processos bioquímics que es troben a la natura com la glucòlisi i el cicle de Krebs. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Mostrar com es poden utilitzar diversos compostos carbonílics per formar enllaços carboni-carboni. S'introdueix el concepte de compostos carbonílics que reaccionen amb ells mateixos: un compost que conté un carbonil actúa com a nucleòfil (a través de l'enolat) i l'altre actúa com a electròfil. Depenent dels diferents compostos carbonílics que utilitzem, obtenim diferents productes. |
|
|
|
| |
Resum de Classe 3.09 |
|
|
|
| |
Reaccions introduïdes: Alquilació a la posició alfa, Condensació aldòlica, Condensació de Claisen, Reacció de Mannich, Nitroaldòlica |
|
|
|
| |
 |
|
|
|
| |
Reaccions de Compostos b-dicarbonílics |
|
|
|
| |
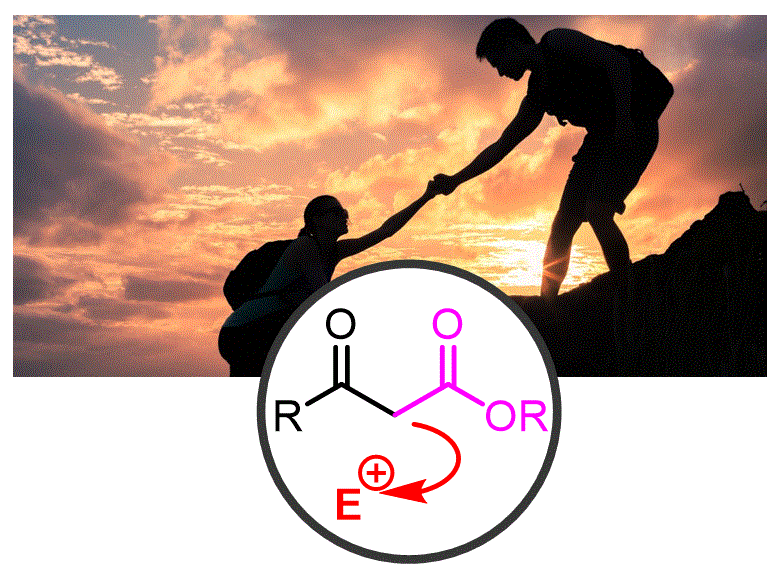
Quan intentem alquilar un enolat sovint ens trobem amb el problema de reaccions addicionals no desitjades que donen lloc a mescles complexes. Si utilitzem un compost carbonílic amb un grup activador adjacent (com un èster) les reaccions són més selectives i controlables. Després de la reacció d'alquilació selectiva, més tard podem eliminar aquest "grup d'ajuda" mitjançant la descarboxilació. Això ens proporciona una manera de sintetitzar cetones i àcids carboxílics en funció del material inicial utilitzat. |
|
|
|
| |
 |
|
|
|
| |
|
|
|
|
| |
Objectiu de Classe: Mostrar com es poden utilitzar grups activadors adjacents als carbonils per alquilar eficaçment compostos carbonílics com ara cetones substituïdes i àcids carboxílics. Mostra com es poden utilitzar els b-ceto èsters per sintetitzar cetones i els èsters malonats per sintetitzar àcids carboxílics. |
|
|
|
| |
Resum de Classe 3.10 |
|
|
|
| |
Reaccions introduïdes: Alquilació de b-cetoèsters, Descarboxilació de b-cetoèsters, Síntesi d’èster acetoacètic, Síntesi Malònica, Reacció de Knoevenagel, Formació de cuprats |
|
|
|
| |
 |
|
|
|
| |
Classe: 3.11: Reaccions i Síntesi de Nitrils |
|
|
|
| |
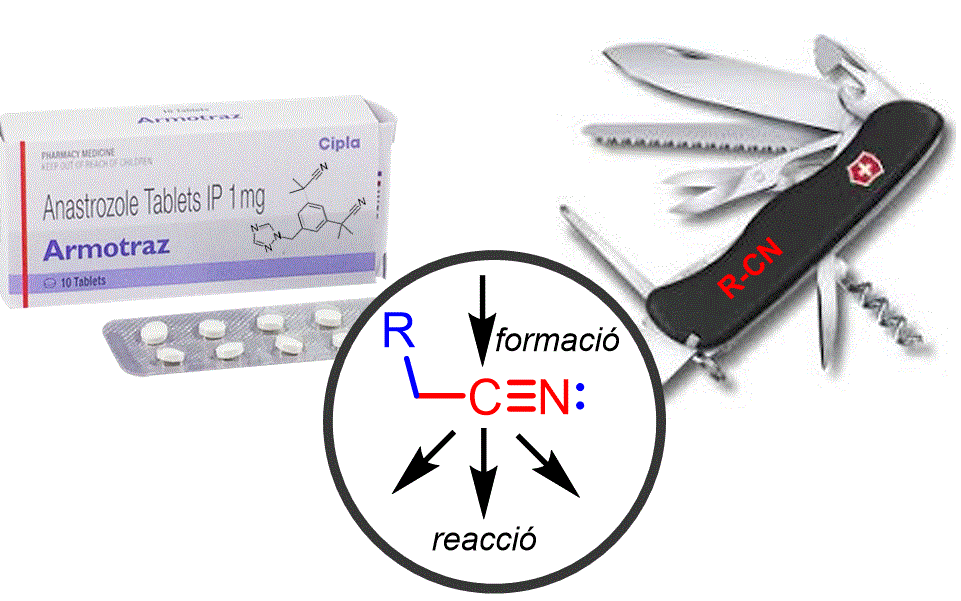
Igual que l'altre compost hibridat sp que vam veure anteriorment (alquins, classe 2.06), el grup nitril no es troba en molts compostos (tot i que hi ha exemples). No obstant això, igual que els alquins, aquest grup funcional és un altre grup útil del tipus "navalla suïssa" que podem utilitzar per aconseguir la síntesi dels grup funcionals més importants com aldehids, cetones, àcids carboxílics i amines. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Discutir les reaccions clau dels nitrils il·lustrant el ventall de reaccions útils que poden experimentar. |
|
|
|
| |
Resum de Classe 3.11 |
|
|
|
| |
Reaccions introduïdes: Hidròlisi de nitrils, Alcohòlisi de nitrils - formació d’èsters, Reducció de nitrils – obtenció d’amines, Alquilació de nitrils, Formació de cianohidrines |
|
|
|
| |
 |
|
|
|
| |
Classe: 3.12: Compostos carbonílics a, b-insaturats |
|
|
|
| |
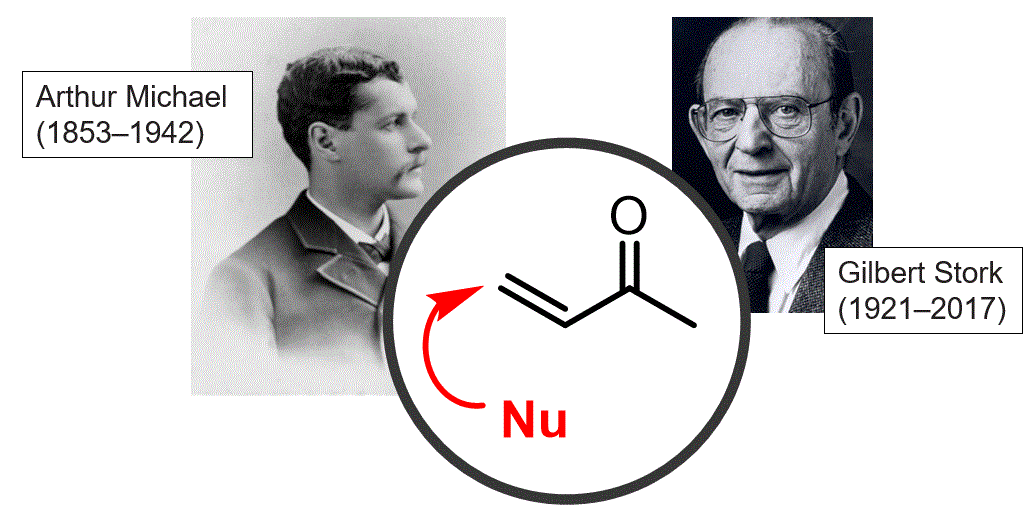
Fins ara hem considerat els alquens com a compostos amb un enllaç pi ric en electrons que actuen com a nucleòfils en les reaccions. En aquesta classe final del curs es mostren exemples en què el paper de l'alquè pot canviar a un electròfil mitjaçant la conjugació de l'alquè amb un grup que retira electrons. L'addició de nucleòfils a aquests alquens deficients d'electrons s'anomena addició de Michael pel seu descobridor. |
|
|
|
| |
 |
|
|
|
| |
Objectiu de Classe: Mostrar com es poden convertir els alquens en electròfils (acceptadors de Michael). Discutir el millor tipus de nucleòfils (donadors de Michael) per reaccionar amb alquens deficients d'electrons. Introduïr una variació que converteixi el carbonil en una enamina i utilitzar-la com a nucleòfil en una reacció de tipus Michael: la reacció de Stork. |
|
|
|
| |
Resum de Classe 3.12 |
|
|
|
| |
Reaccions introduïdes: Reacció de Michael - Addició conjugada 1,4, Enamines - Alquilació de la posició alfa (reacció de Stork), Reacció de Robinson |
|
|
|
| |
 |
|
|
|
| |
|
|
|
|